KMSAuto – удобный в использовании и понятный новичкам активатор Windows и Office. Актуальность данного приложения чрезвычайно высока, так как он позволяет сэкономить значительные средства пользователям ПК по той причине, что лицензионное программное обеспечение и операционная система стоят очень дорого.
Что такое
KMSAuto – маленькая, простая, но в то же время многофункциональная программа, которая способна быстро активировать ОС или пакет офисных программ, подобрав к ним рабочий лицензионный ключ. По факту – это служба управления лицензионными ключами.
Важно, что KMSAuto совершенно безопасно активирует софт и ОС, не нанося вред системе и не внося в нее никаких серьезных изменений. После активации приложение работает в фоновом режиме как отдельная служба и совершенно не мешает системе и не нагружает ее, а потому для юзера она останется незаметной.
Принцип работы
Чтобы понять, как именно работает KMSAuto, требуется понимать, как вообще функционирует проверка на лицензию операционной системы. В самой ОС Windows установлена служба, которая регулярно собирает данные и отправляет их на сервер, где они анализируются и проводится проверка на лицензию.
В пиратской версии такая проверка всегда заканчивается отказом со стороны сервера и по итогу владелец ПК видит постоянное уведомление, что его система не активирована и по итогу он не может использовать весь ее функционал, а также не может быть уверен в безопасности своих данных.
Пароль: 2024
Говоря о принципе работы KMSAuto, стоит сказать, что программа создает в ОС Windows службу, которая имитирует собой подлинную и посылает якобы подлинные данные на сервер о том, что пользователем была куплена лицензия, то есть была произведена активация. Эта служба, как уже говорилось, работает постоянно и не мешает работе системы.
Особенности KMSAuto
KMSAuto на данный момент является лучшим активатором и в разы превосходит аналоги по своему функционалу и по удобству в использовании.
Говоря о достоинствах KMSAuto, также стоит выделить:
- Поддержка серверных систем 2008-2016 года.
- Активация практически всех операционных систем от Microsoft, включая Windows 7, 8, 10, 11, а также Vista (работает не идеально).
- Активация Office.
- Работает на 32-битных и на 64-битных системах.
- Присутствует крайне полезная функция удаления истории предыдущих попыток активации и истории обновлений – они мешают последующим активациям.
- Есть возможность заменить домашнюю версию Windows на профессиональную и максимальную.
Разновидности KMSAuto
KMSAuto – это полезный, но не универсальный инструмент, который подойдет к каждой ОС. Всего разработано три версии данной утилиты под определенные нужды пользователей:
- Ultimate – используется для активации новых операционных систем, включая Windows 8, 10 и 11, а также для пакета офисных программ. Может похвастаться наибольшим функционалом и количеством инструментов.
- Lite – облегченная версия, которая также применяется для активации Windows 8, 10 и 11, а также офисных программ. Однако ее не нужно устанавливать на ПК и для ее работы не требуется Фреймворка. Количество инструментов в ней также несколько меньшее.
- Helper – программа для активации старых операционных систем, в особенности Windows7 и Vista. Однако с помощью нее можно активировать любые версии Office.
Как активировать
В случае KMSAuto предусмотрено как минимум 2 метода активации. Первый из них – автоматический и является наиболее простым, но в то же время и не универсальным. Второй – ручной, более сложный, но универсальный. Ниже рассмотрим оба метода.
Автоматическая активация
Для автоматической активации не потребуется никаких глубокий знаний работы с подобным софтом.
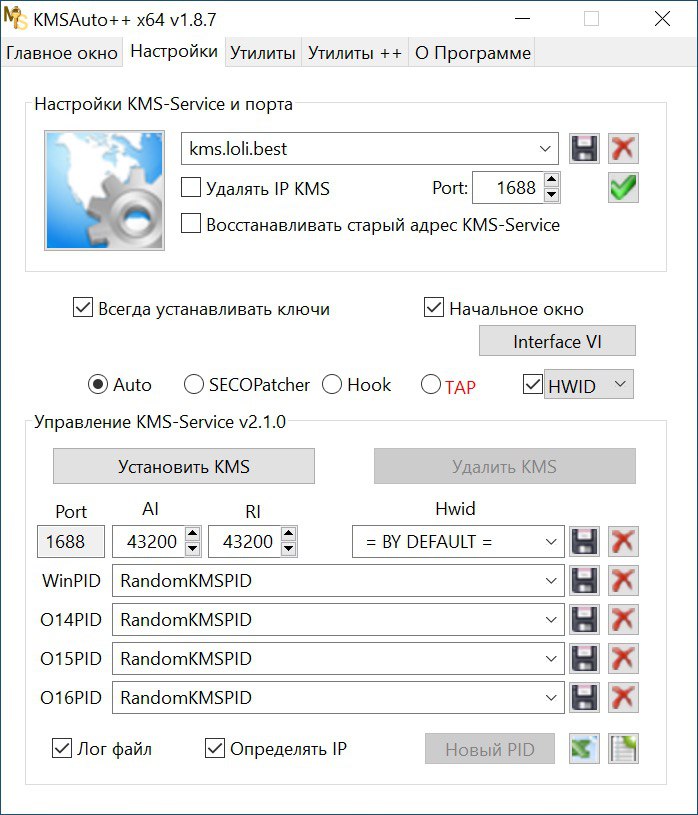
Однако стоит отметить крайне важный момент – автоматический метод работает только в том случае, если юзер ранее не пытался активировать систему и на нее не устанавливались обновления.
Инструкция для автоматической активации:
- Отключить антивирусную программу.
- Запустить KMSAuto от имени администратора.
- Выбрать, что именно требуется активировать.
- Разрешить установку и дождаться ее завершения.
- Перезагрузить компьютер.
Ручная активация
Ручной метод нужен в особенности тем, кто уже пытался ранее активировать систему или на нее уже устанавливались обновления.
Инструкция для ручной активации:
- Запустить KMSAuto от имени администратора, предварительно отключив антивирус.
- Перейти во вкладку «Утилиты».
- Нажать на «Установить GVLK-ключ».
- Выбрать систему или программу, которую нужно активировать.
- Из появившегося списка выбрать и скопировать GVLK-ключ.
- Перейти во вкладку «Система» и нажать на «Установить GVLK-ключ», после чего в поле вставить скопированный ранее ключ и нажать «Далее».
- Дождаться завершения установки и перезагрузить ПК.
Почему не получается активировать
Во время работы с KMSAuto у пользователей могут возникнуть проблемы – программа порой выбивает ошибку, из-за которой нельзя успешно завершить установку.
К счастью, причин, почему появляется ошибка – немного и что еще круче – они с легкостью решаются.
Причины ошибок и их решение:
- Не используется актуальная версия KMSAuto – для того, чтобы работать с последними сборками Windows важно применять современные версии активатора, иначе заполучить лицензию и не выйдет.
- Процесс активации блокирует антивирус – это нормальная реакция на KMSAuto, и решить эту проблему можно, просто отключив на время антивирус.
- Данная версия KMSAuto не подходит для конкретной ОС Windows – стоит выбирать ту сборку, которая подходит к определенной системе.
- Ошибка при активации ключа – в этом случае требуется попробовать еще один метод установки (через режим GVLK).
Вывод
Правильное использование приложения KMSAuto позволит быстро и безопасно активировать ОС Windows и программы Office. Удобство и простота позволяют даже новичку заполучить лицензию без особых проблем.
Главное – действовать исходя из инструкции и предварительно подготовиться, выбрав правильную сборку KMSAuto и отключив антивирус.